В чем сложность замены импортного медицинского ПЭЭК для имплантатов отечественной продукцией?
После 20 лет бурного развития отечественная ортопедия постепенно сломала монополию иностранных товаров. Однако, что касается основных биомедицинских материалов, некоторые отечественные материалы по-прежнему находятся в затруднительном положении.
Таким материалом является PEEK (полиэфирэфиркетон) для медицинских имплантатов. За последние несколько десятилетий материал PEEK для имплантатов был монополизирован тремя производителями в мире, поэтому нам приходится принимать дорогостоящее сырье из-за границы. Некоторые иностранные марки материалов даже не продаются на китайский рынок, и купить их по высоким ценам не представляется возможным, не говоря уже о централизованных закупках с уменьшением объема и цен.
Нарушение монополии на импортные материалы для медицинских имплантатов всегда было целью и мечтой отечественных предприятий. Однако почему отечественным предприятиям на протяжении стольких лет было трудно прорвать зарубежную блокаду? После многолетних исследований и обобщений можно выделить четыре основные трудности:
1. Трудно обновлять производственное оборудование и окружающую среду.
В настоящее время в Китае около 5 производителей имеют возможность проводить полимеризацию PEEK промышленного уровня, и почти все из них разработали зрелые процессы и оборудование для полимеризации PEEK промышленного уровня. Поскольку эти компании, производящие PEEK, развивались раньше, им трудно удовлетворить производственные требования PEEK для имплантатов с точки зрения компоновки производственной среды, производственного оборудования и связанных с ним конфигураций.
Большинство отечественных поставщиков сырья PEEK не имеют квалификации для производства медицинских изделий, а соответствующие требования и стандарты для линий по производству имплантатов не ясны. В то же время химическим компаниям очень сложно менять оборудование и производственные линии, и они испытывают большое финансовое давление. На изучение и создание новых производственных линий уходит много времени.

2. Процесс очистки имплантируемого ПЭЭК сложен.
From the product point of view, there is little difference in performance between industrial PEEK and implantable PEEK. The main difference lies in the purity of the material. To ensure the biocompatibility of PEEK materials for long-term use in the human body, it is necessary to ensure that the content of some trace chemical elements and heavy metal ions in them does not exceed the standard. At present, almost all PEEK produced by domestic enterprises has the problem of excessive content of trace elements and metal ions.
At present, this problem can only be dealt with during the polymerization and refining process, and it is difficult to remove it even with high-pressure melt filtration in the subsequent granulation. To solve this problem, PEEK manufacturers need to actively work with domestic equipment manufacturers to jointly develop equipment that meets the requirements of implant PEEK refining and purification, and study new purification processes. Only by making breakthroughs in both equipment and process can we ensure the effective removal of metal ions and trace chemicals during purification.
3. Material and process compliance is difficult
Making products is only the first step, and complying with YY/T 0660-2008 and 16886 related implant materials is only the basic requirement. As a domestic head implant grade PEEK material manufacturer, when submitting product registration, it will definitely be strictly reviewed by the review teacher, and the Food and Drug Administration will even conduct a surprise inspection of the entire production process. The production enterprise must at least have key process flows such as polymerization, refining, granulation, and extrusion.
How to demonstrate to the judges the stability and reliability of the process throughout the entire production process, and how to demonstrate the traceability of the entire production and processing and manufacturing process are both very important and difficult.
4. Acceptance and recognition still requires process
It will take time for government regulatory agencies, medical device companies and hospital doctors to accept and recognize domestic materials.
As one of the earliest domestic companies engaged in the research, development, production and manufacturing of PEEK materials, Jiangsu Junhua pays great attention to the application of PEEK in the medical industry and has been committed to the research, development and production of medical implant-grade PEEK materials.
After 16 years of production and technology accumulation, the company started from the source of polymerization and established Shandong Junhao High Performance Polymer Co., Ltd. to polymerize implantable PEEK raw materials. According to the production standards of medical implant materials, a GMP refining production workshop was established, and professional refining and purification equipment for implantable AKSOPEEK polymerization was developed, which effectively solved the problem of excessive heavy metal ion content in implantable PEEK materials.

In order to further effectively realize full-process monitoring and traceability, the company selected a DCS central control system, which can effectively realize the control and detection of the main parameters inside the equipment during the production process, ensure that the production process is fully controllable, and the production data can be archived separately for subsequent traceability.

The company pilot-produced autoclave-grade PEEK materials in 2020. In the same year, third-party tests were conducted on various biological aspects of the materials in accordance with the ISO10993 test standard, and all test results met the requirements.
In 2021, the first batch of mass-produced implantable AKSOPEEK materials will be sent for testing of biological and physical and chemical properties in accordance with the YY/T0660-2008 medical industry standard. It is expected that all tests will be completed around September 2022, and the filing of the master file with the State Food and Drug Administration is planned to be completed in the same year.
Junhua PEEK uses an ICP (Inductively Coupled Plasma) instrument to test metal ions, and the lead ion content is extremely low, less than 0.002%.
In addition to the basic requirements for implantable products, the main concern of customers is the mechanical properties of PEEK products, which are related to whether patients can use them for a long time.
In response to the requirements of mechanical properties, Junhua PEEK has developed high-toughness AKSOPEEK, which guarantees the patient’s postoperative recovery with performance far exceeding the standards.
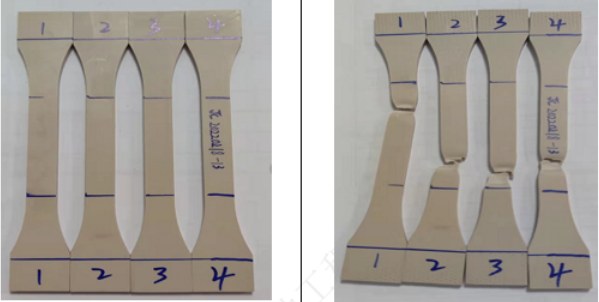
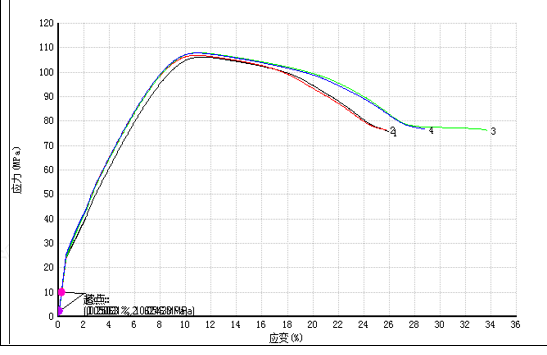
In addition, when we use implant-grade PEEK, there are also relevant medical industry testing specifications for certain specific uses, the most representative of which is the intervertebral fusion device.
Используя стандартный метод испытаний механических свойств межпозвонкового спондилодеза спинальных имплантатов YY/T 0959 (ASTM F2077), устройство для межпозвонкового спондилодеза AKSOPEEK Natural (H = 6,3 мм) было подвергнуто испытаниям на усталость при сжатии при нагрузке 2000/4000 Н, частота 5 Гц и количество испытаний 5 миллионов раз. Никаких сбоев из-за усталости не произошло. Статические испытания до и после усталости также не показали какого-либо снижения прочности, и эта модель термоядерного устройства показала предел прочности при сжатии только при 12000 Н.



